Ausschuss für Verpackung und Kennzeichnung der ADKA und Arbeitsgruppe Onkologie im Ausschuss Klinische Pharmazie der ADKA
Injektions- und Infusionsflaschen, die Zytostatika enthalten, sind teilweise produktionsbedingt auf den äußeren Oberflächen mit Wirkstoff kontaminiert. Dies wird als eine der Ursachen der Kontamination von Arbeitsplätzen und Arbeitsplatzumgebungen mit Zytostatika diskutiert. Eine Gesundheitsgefährdung des Personals kann nicht ausgeschlossen werden.
Zum Schutz der Beschäftigten steht der Hersteller in der Pflicht, seine Herstellprozesse so auszurichten, dass Außenkontaminationen von Primär- und Sekundärverpackungen mit Zytostatika so weit wie möglich vermieden werden. Als ergänzende Maßnahme können Schutzverpackungen eingesetzt werden, um eine Kontamination durch Kontakt mit den Oberflächen und eine Verschleppung der Kontamination zu verhindern. Zudem können Schutzverpackungen dazu beitragen, Glasbruch zu vermeiden.
Bevor die Zytostatika in den Zubereitungsbereich – die Sicherheitswerkbank oder den Isolator (Reinraumklasse A) – eingebracht werden, müssen die Behältnisse desinfiziert werden, um aseptische Bedingungen zu gewährleisten. In der Regel wird eine Wischdesinfektion der Oberflächen durchgeführt. Dabei genügt es, die Schutzverpackung zu desinfizieren. Würden die Primärbehältnisse aus der Schutzverpackung entnommen, wäre sowohl der Kontaminationsschutz als auch der Bruchschutz aufgehoben. Keimfreiheit kann für die Innenseiten der Schutzbehältnisse und die Außenseiten der Injektionsflaschen nicht angenommen werden; eine Kontamination durch an der Innenseite des Schutzbehälters haftende Erreger ist aber bei der Entnahme aus dem Primärbehältnis ohne Entfernung des Schutzbehältnisses nicht zu erwarten.
Für die Desinfektionsmaßnahme müssen sowohl die Erfordernisse des Arbeitsschutzes als auch die Erfordernisse der aseptischen Zubereitung berücksichtigt werden. Zur Desinfektion wird das Wischverfahren empfohlen. Bei der Sprühdesinfektion besteht die Gefahr, dass zu viel Desinfektionsmittel aufgebracht wird und der Überschuss abtropft oder dass zu wenig Desinfektionsmittel aufgebracht und die Oberfläche nicht komplett desinfiziert wird. Zudem ergibt die Reibung beim Wischvorgang eine bessere Desinfektionsleistung.
Wir empfehlen daher folgendes Vorgehen zur Desinfektion von Injektionsflaschen, die CMR-Wirkstoffe enthalten und in Schutzbehältern verpackt sind (CMR: kanzerogen, mutagen, reproduktionstoxisch):
1. Ein nicht faserndes Tuch/Vlies wird mit ausreichend Desinfektionsmittel satt getränkt. Das Desinfektionsmittel soll nicht abtropfen.
2. Die gesamte Außenseite des Schutzbehälters, das heißt Boden, Deckel und Körper, werden damit desinfiziert.
3. Der Deckel wird abgeschraubt bzw. entfernt, ein Tupfer mit Desinfektionsmittel getränkt und der dann erreichbare Gewindebereich am Behälterkörper wischdesinfiziert.
4. Der Bereich des Glasfläschchens, der jetzt freiliegt und im Laufe der Zubereitungstätigkeiten berührt werden kann – das sind Flaschenbrust und -hals sowie die Flipp-off-Kappe –, wird desinfiziert.
5. Nach dem Entfernen der Flip-off-Kappe wird die Einstichstelle des Gummistopfens desinfiziert.
6. Unter Beachtung der Einwirkzeit des Desinfektionsmittels wird der Stopfen mit einem Entnahmespike durchstochen.
7. Entleerte Vials werden komplett zusammen mit dem Schutzbehälter entsorgt.
Die einzelnen Schritte sind in den Abbildungen 1 bis 7 dargestellt.

Ein nicht faserndes Tuch/Vlies wird mit Desinfektionsmittel satt getränkt. [alle Fotos: Dr. Werner Kittlaus, Pullach]
1

2
Alle Außenflächen, das heißt Boden, Umfang und Deckel des Schutzbehälters, werden wischdesinfiziert.
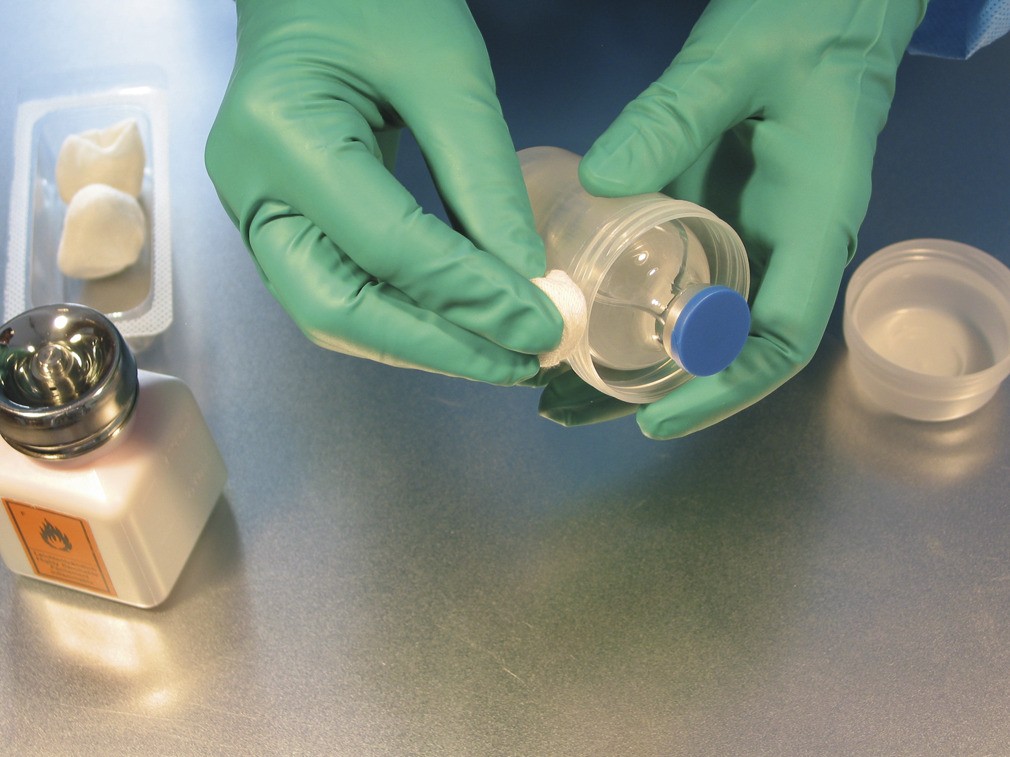
Der Deckel wird abgeschraubt bzw. entfernt, ein Tupfer mit Desinfektionsmittel getränkt und das dann freiliegende Gewinde wischdesinfiziert.
3

Flaschenbrust und -hals sowie die Flip-off-Kappe werden desinfiziert.
4

Nach Entfernen der Flip-off-Kappe wird die Einstichstelle des Gummistopfens desinfiziert.
5

Nach Verstreichen der Einwirkzeit des Desinfektionsmittels wird der Stopfen mit einem Entnahmespike durchstochen.
6

Das Glasvial wird nach Gebrauch komplett zusammen mit dem Schutzbehälter entsorgt.
7
Wichtig: Das Vial darf nicht aus dem Schutzbehälter entnommen werden!
Krankenhauspharmazie 2011; 32(01)
