Hardy-Thorsten Panknin, Berlin, Prof. Dr. med. Matthias Trautmann, Stuttgart
In den Jahren 2008 und 2012 hat die Surviving Sepsis Campaign Empfehlungen zum Sepsismanagement in der Notaufnahme und auf der Intensivstation publiziert [1, 2]. Einer der wichtigsten Bausteine ist dabei eine frühzeitige, empirische Antibiotikatherapie, die unmittelbar nach der Abnahme von Blutkulturen beginnen sollte. Weitere Bestandteile sind die Bestimmung des Serumlactat-Werts, die Messung der hämodynamischen Parameter und die Ermittlung der Sauerstoffsättigung. Die Messwerte dienen dazu, supportive intensivmedizinische Maßnahmen einzuleiten und zu steuern. Die chirurgische Diagnostik und Herdsanierung wird in den Empfehlungen der Sepsiskampagne jedoch nur kurz thematisiert. Die Autoren aus Gießen geben hierzu detaillierte Empfehlungen ab [3].
Fokus im Bauchraum häufigste Ursache
Bezogen auf alle Fälle von schwerer Sepsis ist ein Sepsisherd im Bauchraum mit 66% die häufigste Ursache. Betrachtet man lediglich Patienten, bei denen die Sepsis nach einem größeren bauchchirurgischen Eingriff auftrat, so liegt sogar in 85% der Fälle ein intraabdomineller Fokus wie beispielsweise eine Nahtdehiszenz mit sekundärer Peritonitis vor. Die Autoren betonen, dass an eine solche Komplikation auch dann gedacht werden muss, wenn sich der Patient nach einer Operation zunächst nicht in der chirurgischen Notaufnahme, sondern beim niedergelassenen Arzt bzw. in der Allgemeinsprechstunde vorstellt. Gerade bei älteren Patienten kündigt sich eine postoperative Sepsis oft mit unspezifischen Allgemeinbeschwerden an. Solche Beschwerden können eine Oligurie (maskiertes Schocksyndrom) oder ein geistiger Leistungsabfall sein.
Sehr wichtig ist es, in diesem Stadium eine laborchemische Bestimmung des C-reaktiven Proteins (CRP) durchzuführen. Nach Pankreaseingriffen signalisiert beispielsweise ein CRP-Wert von >140 mg/dl am vierten Tag nach der Operation eine entzündliche Komplikation. Klinisch sollte unbedingt auf die Atemfrequenz geachtet werden, die bei systemisch wirksamen Entzündungsprozessen deutlich über den Normwert von 12 Atemzügen pro Minute in Ruhe erhöht ist. Bei erhöhter Atemfrequenz kann die Pulsoxymetrie wertvolle Hinweise geben. Liegt der damit gemessene Wert der Sauerstoffsättigung unter 90%, sollte schnellstmöglichst eine weitere Diagnostik eingeleitet werden.
Schnelle Diagnostik mit Ultraschall, gefolgt vom CT
Ist der Verdacht auf eine Komplikation im Bauchraum einmal festgestellt, so sollte bereits in der Notaufnahme bzw. in der Ambulanz eine abdominelle Ultraschalluntersuchung vorgenommen werden. Sie kann Hinweise auf einen Abszess oder freie Flüssigkeit im Bauchraum geben. Genauere Informationen liefert die computertomographische Untersuchung (CT), während das abdominelle MRT (Magnetresonanz-Tomogramm) weniger gut für die Erkennung entzündlicher Prozesse geeignet ist.
Gibt die Bildgebung Hinweise auf einen entzündlichen Sepsisherd, sollte die operative Sanierung baldmöglichst angestrebt werden. Die Autoren unterstreichen jedoch, dass ein optimales Zeitfenster für einen solchen Eingriff innerhalb des ersten Tages nach Aufnahme wissenschaftlich nicht exakt definiert wurde. Der Effekt eines verzögerten Vorgehens (Verzögerung >24 bzw. >48 Stunden) wurde in mehreren Studien evaluiert. In einer Studie bei Patienten mit akutem Abdomen lag beispielsweise die Letalität bei 27%, wenn innerhalb von 48 Stunden operiert wurde, während sie bei späterer OP auf 59% stieg. Bei perforierten Magenulzera zeigte sich in einer Studie ein Anstieg der Letalität um 2,4% für jede Stunde der Verzögerung eines operativen Eingriffs. Es hat daher Sinn, den operativen Eingriff so früh wie möglich am Tag der Diagnosestellung einer Sepsis mit operativ sanierbaren Fokus einzuplanen.
Aus einer groß angelegten klinischen Studie ist bekannt, dass Patienten mit der Diagnose einer Sepsis umgehend auf die Intensivstation verlegt werden sollten. In der Studie zeigte sich ein Anstieg des Mortalitätsrisikos um 1,5% für jede Stunde, um welche die Verlegung auf die Intensivstation verzögert wurde [4].
Chirurgischer Eingriff: In der Sepsis so begrenzt wie möglich
Das operative Vorgehen hat zum Ziel, den Eiterherd zu drainieren und eine vorhandene Leckage oder Dehiszenz zu schließen. Der Eingriff sollte sich in der akuten Sepsisphase möglichst auf essenzielle Maßnahmen beschränken. Die Herstellung physiologischer anatomischer Verhältnisse ist ein späteres Ziel, welches nach Stabilisierung des Patienten in einem Revisionseingriff in Angriff genommen werden kann. Eine Frage, die im Rahmen der chirurgischen Forschung der vergangenen Jahre immer wieder evaluiert wurde, ist die, ob nach einem Ersteingriff geplante Relaparotomien (sog. „second-look“-OP) zu definierten Zeitpunkten vorgenommen werden sollen, oder ob sich die Notwendigkeit eines erneuten Eingriffs an klinischen Befunden und Symptomen orientieren sollte („on-demand“-Relaparotomie). In einer Studie mit großer Patientenzahl (116 pro Gruppe) konnte gezeigt werden, dass sich die Mortalität bei „on-demand“-Relaparotomie nicht erhöhte, während die Anzahl der chirurgischen Interventionen und der Verbrauch von Krankenhausressourcen signifikant geringer war [5].
Die Autoren weisen allerdings auf zwei Indikationen hin, bei denen eine geplante Relaparotomie sinnvoll ist. Zum einen sollte ein solcher Eingriff am Folgetag eingeplant werden, wenn sich bei der Erst-OP Hinweise für eine Darmischämie ergaben. Hier muss bei dem zweiten Eingriff überprüft werden, ob weitere Darmanteile minderdurchblutet oder gar bereits nekrotisch geworden sind. Eine Indikation zum geplanten Zweiteingriff besteht auch, wenn die vordere Bauchwand wegen massiver Distension der Darmschlingen nicht geschlossen werden konnte. Dass insgesamt eine erfolgreiche Sanierung eines intraabdominellen Infektionsherds die Prognose des Sepsispatienten erheblich verbessern kann, ergab sich aus einer Reihe von vergleichenden Kohortenstudien (Tab. 1).
Tab. 1. Bedeutung der chirurgischen Fokussanierung für die Mortalität des Sepsispatienten [3]
|
Erstautor, |
Erkrankung |
Patienten [n] |
Initiale Fokussanierung nicht gelungen [%] |
Mortalität [%] |
|
|
Bei primär gelungener Fokussanierung |
Bei primär nicht gelungener Fokussanierung |
||||
|
Anderson et al., 1996 |
Schwere intraabdominelle Sepsis |
125 |
48 |
19,2 |
90,2 |
|
Büchler et al., 1997 |
Diffuse Peritonitis |
186 |
11 |
10 |
25 |
|
Wacha et al., 1999 |
Diffuse Peritonitis |
355 |
30 |
14 |
47 |
|
Seiler et al., 2000 |
Diffuse Peritonitis |
258 |
11 |
13 |
27 |
|
Barie et al., 2004 |
Intraabdominelle Infektionen |
465 |
? |
Anstieg um 22,6% |
|
Mikrobiologie: Proben aus dem Bauchraum sind unverzichtbar
Bei der Exploration des Bauchraums sollten aus dem Sepsisherd sowie aus weiteren Materialien wie Aszitesflüssigkeit oder entzündlich verändertem Gewebe Proben für die mikrobiologische Untersuchung abgenommen werden. Dies sollte auch dann geschehen, wenn der Patient bereits eine Antibiotikatherapie erhält. Dass Letztere möglichst früh begonnen werden sollte, ist heute Standardwissen. Die Untersuchung der Materialien aus dem Bauchraum kann dennoch dazu dienen, Erreger nachzuweisen, die nicht im Spektrum der initial eingesetzten antimikrobiellen Pharmaka liegen.
Neben der konventionellen Diagnostik werden zunehmend auch molekulare Techniken wie der Erregernachweis mittels Amplifikation der 16S rDNA eingesetzt, die allerdings nur in spezialisierten Laboratorien zur Verfügung stehen. Die Autoren erwähnen auch den Schnelltest auf bakterielle Erreger mit dem SeptiFast-System (einer breit angelegten Technik auf der Basis der Polymerase-Kettenreaktion), die allerdings lediglich für Blutproben validiert ist. Auch sie ermöglicht einen Erregernachweis selbst dann noch, wenn bereits eine breit wirksame antibiotische Therapie begonnen wurde.
Sepsisbündel als Checkliste
Für den schnellen Gebrauch am Krankenbett haben die Autoren aus den von der Sepsis Campaign publizierten Maßnahmenbündeln eine Checkliste erstellt, die mit Zeitvorgaben versehen ist. Man kann daran ersehen, dass die chirurgische Intervention in der Maßnahmenkette erst an dritter Stelle steht, mit unklarer Aussage über den Einfluss der Dauer bis zur chirurgischen Intervention auf die Prognose (Abb. 1). Hämodynamische und respiratorische Stabilisierung des Patienten haben in jedem Fall Vorrang. Eine eventuell sinnvolle niedrig dosierte Glucocorticoid-Therapie bei ungenügendem Ansprechen des Patienten auf Catecholamine steht am Ende der Handlungskette.
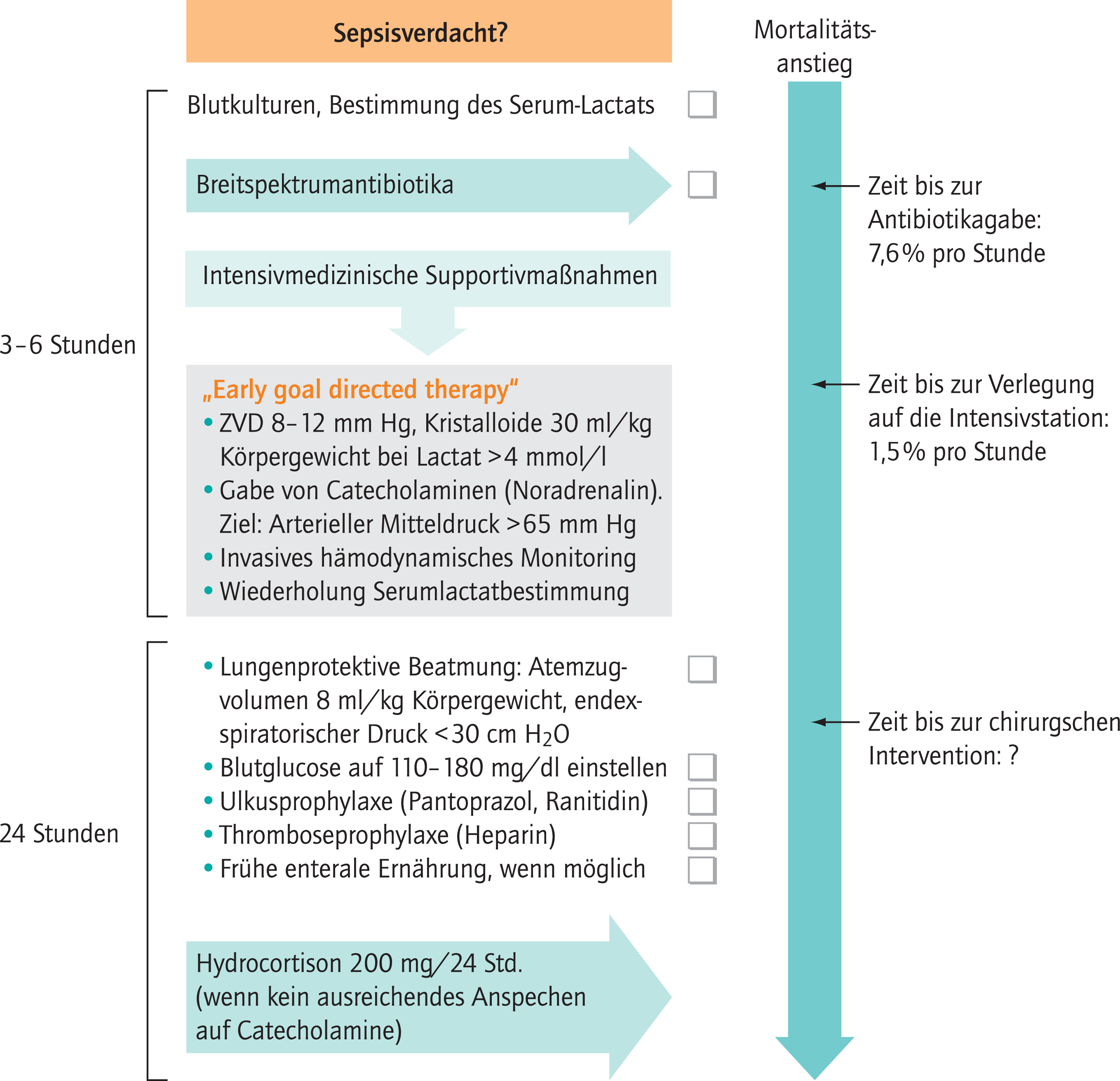
Abb. 1. Checkliste für das Management der schweren Sepsis innerhalb der ersten 24 Stunden. Early goal directed therapy: Frühe, an Behandlungszielen ausgerichtete Intensivtherapie; Behandlungsziele sind: arterieller Mitteldruck >65 mmHg, gemischtvenöse Sauerstoffsättigung ≥70%, zentraler Venendruck (ZVD) 8–12 mmHg [mod. nach 3]
Kommentar
Die Leitlinien der internationalen Sepsiskampagne thematisieren in der Tat vor allem intensivmedizinische und pharmakotherapeutische Aspekte des Sepsismanagements, während die chirurgische Herdsanierung lediglich stichwortartig erwähnt wird. In der vorliegenden Übersichtsarbeit werden deshalb wichtige Punkte zum chirurgischen Vorgehen ergänzt. Die Autoren stellen anhand der zitierten Literaturstudien überzeugend dar, dass programmierte Relaparotomien, wie sie früher üblich waren, heute nicht mehr als Stand der Wissenschaft gelten können. Dass eine operative Sanierung eines vermuteten intraabdominellen Sepsisherds zwingend geboten ist, dürfte unstrittig sein. Der optimale Zeitpunkt für diesen Ersteingriff wurde jedoch nicht in prospektiven Studien geklärt. Diese verbieten sich auch aufgrund ethischer Überlegungen. Es ist sinnvoll, wie von den Autoren empfohlen, zunächst die hämodynamische Stabilisierung des Patienten abzuwarten, ehe ein Transfer in den Operationssaal erfolgt.
Die Autoren konzentrieren sich auf abdominalchirurgische Eingriffe, während die Extremitätenchirurgie in der Arbeit nur am Rande erwähnt wird. Dabei sind ausgedehnte Haut- und/oder Weichgewebeinfektionen durchaus nicht selten Ursache eines schweren Sepsisgeschehens. Ein klassisches Krankheitsbild ist der Gasbrand nach verschmutzten Verletzungen, beispielsweise im Straßenverkehr. Auch die nekrotisierende Fasziitis durch A-Streptokokken stellt eine Indikation zur operativen Revision mit Dekompression der Faszienlogen und Entfernung nekrotischen Gewebes dar. Auch für diese Erkrankungen gilt, dass bei operativer Freilegung des infizierten Gebiets unbedingt mikrobiologische Proben gewonnen werden müssen. Leider werden allzu häufig lediglich Abstriche genommen, während das reichlich vorhandene Gewebsmaterial oder der Eiter nicht eingesandt werden. Sofern die letztgenannten Materialien aus der Tiefe des Gewebes ohne Hautkontakt gewonnen werden können, hat es durchaus Sinn, sie in ein Blutkulturfläschchen zu überimpfen. Dadurch gelingt oft noch eine Anzüchtung des verursachenden Erregers, auch wenn bereits eine Antibiotikatherapie begonnen wurde. Bei Verdacht auf Gasbrand muss die Probe in ein anaerobes Medium (z.B. Thioglykolat-Bouillon) eingebracht und möglichst umgehend ins Labor transportiert werden.
Literatur
1. Dellinger RP, et al. Surviving sepsis campaign: International guidelines for management of severe sepsis and septic shock: 2012. Crit Care Med 2013;41:580–637.
2. Dellinger RP, et al. Surviving sepsis campaign: International guidelines for management of severe sepsis and septic shock: 2008. Crit Care Med 2008;36:296–327.
3. Hecker A, et al. Diagnostics, therapy and outcome prediction in abdominal sepsis: current standards and future perspectives. Langenbecks Arch Surg 2014;399:11–22.
4. Cardoso LT, et al. Impact of delayed admission to intensive care units on mortality of critically ill patients: a cohort study. Crit Care 2011;15:R28.
5. Van Ruler O, et al. Comparison of on-demand vs. planned relaparotomy strategy in patients with severe peritonitis: a randomized trial. JAMA 2007;298:865–72.
Prof. Dr. med. Matthias Trautmann, Stuttgart
Krankenhauspharmazie 2014; 35(06)
